I. REACCIONES Y ECUACIONES QUÍMICAS
- PUNTO DE PARTIDA: EXPERIENCIA EFECTOS PIROTÉCNICOS DE LA LUZ ( SOLO SE HACE EN CLASE NO EN CASA SIN LA PRESENCIA DEL MAESTRO) ENLACE: REACCIONES Y ECUACIONES QUÍMICAS
- TEMAS A TRATAR EN QUÍMICA: Cambios químicos y físicos, reacción química ( concepto y clases), Ecuaciones( Condiciones de representación, balanceo por tanto y óxido reducción)Estequiometria( interpretación de la ecuación, cálculos químicos de reaccionantes y producto, reactivo limitante y rendimiento de una reacción). MATERIAL ESTEQUIOMETRIA. EJERCICIOS ESTEQUIOMETRIA
- TEMAS A TRABAJAR EN FÍSICA: Calor y temperatura( conceptos, escalas de temperatura, conducción , convección, radiación y longitudes de Onda. ( Link: CALOR Y TEMPERATURA)
- TEMAS A TRABAJAR EN BIOLOGÍA: Temperatura corporal (link: TEMPERATURA CORPORAL)
- TEMAS A TRABAJAR EN CIENCIA , TECNOLOGÍA Y MEDIO AMBIENTE: Efectos del calor a los móviles A. Link: http://www.tuexpertomovil.com/2015/07/03/el-calor-afecta-mucho-mas-de-lo-que-crees-a-tu-movil/ B. http://www.agenciasinc.es/Noticias/Un-nuevo-nanofluido-mejora-un-30-la-conductividad-del-calor
 2. PUNTO DE PARTIDA: Preparación de un jugo de parchita ( chinola, fruta de la pasión, maracuyá, mburucuyá, parcha, parchita, pasionaria) en dos formas diferentes
2. PUNTO DE PARTIDA: Preparación de un jugo de parchita ( chinola, fruta de la pasión, maracuyá, mburucuyá, parcha, parchita, pasionaria) en dos formas diferentes
a) Coloque los gramos de pulpa que desee del interior de la fruta en un vaso o recipiente y agregue primero el volumen de agua que desee, agite y luego adicione la cantidad de azúcar adecuada al gusto . ( Tome datos) b) Coloque otra cantidad en gramos diferente a la anterior de pulpa del interior de la fruta en un vaso o recipiente y agregue primero el azúcar, remueva y luego adicione la cantidad de agua igual al punto 1. Responda a). Cuales son las pruebas organolépticas para la evaluación del producto final. ¿Cuál propiedad coligativa es responsable de lo observado? Exprese las concentraciones de los ingredientes. COLIGATIVA: Los líquidos tienen propiedades físicas características como: densidad, ebullición, congelación y evaporación, viscosidad, capacidad de conducir corriente, etc. Para estas propiedades cada líquido presenta valores característicos constantes. Cuando un soluto y un disolvente dan origen a una disolución, la presencia del soluto determina la modificación de estas propiedades con relación a las propiedades del solvente puro.Propiedades de las disoluciones:
1. propiedades constitutivas: aquellas que dependan de la naturaleza de las partículas disueltas. Ej. viscosidad, densidad, conductividad eléctrica, etc.2. Propiedades coligativas: dependen del número de partículas disueltas en una cantidad fija de disolvente y no de la naturaleza de estas partículas. Ej. Descenso de la presión de vapor, aumento del punto de ebullición, disminución del punto de congelación, presión osmótica. - TEMAS A TRATAR EN QUÍMICA: disolución, clases, ejemplos de disoluciones, tipos de enlaces, componentes de una solución, formas físicas y químicas de expresar la concentración de una disolución. a. Vídeo: https://www.youtube.com/watch?v=x52MbRu-tYA b. Contenidos y ejercicios: http://www.quimicayalgomas.com/quimica-general/estequiometria-y-soluciones-quimicas/soluciones-quimicas/ para entender mejor Normalidad: http://www.quimicas.net/2015/05/ejemplos-de-normalidad.html
- LINK PARA ESTUDIAR MEDIANTE TALLER: guia-de-soluciones-talleres-y-teoria
- TEMAS A TRATAR EN FÍSICA: El efecto tyndal. Como se descubrió el efecto invernadero https://www.xatakaciencia.com/fisica/que-es-el-efecto-tyndall
- TEMAS A TRATAR EN BIOLOGÍA: Fenómenos de transporte a través de la membrana. Presentación contenidos:Transporte a través de las membranas
- TEMAS A TRATAR EN CIENCIA, TECNOLOGÍA Y MEDIO AMBIENTE: Riesgos del uso de soluciones químicas Link: http://www.paritarios.cl/especial_riesgo_uso_productos_quimicos.htm

- PUNTO DE PARTIDA: MAPA

- LECTURA : Variables para el estudio de los gasesVOLUMEN : Indica todo el espacio que ocupa un gas en su movimiento, es decir el volumen de un gas es simplemente el del recipiente en que se encuentre dicho gas.
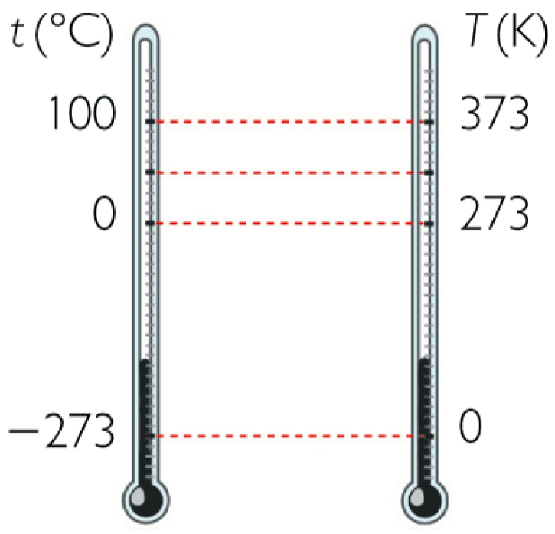
TEMPERATURA: La temperatura mide la intensidad de calor, La temperatura de los gases se mide generalmente en grados centígrados. Cuando se aplican las leyes de los gases ideales, esta temperatura debe convertirse a la escala de Kelvin.
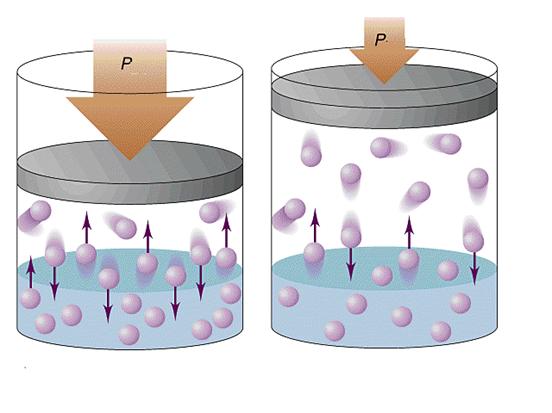
- PRESIÓN: Las moléculas de un gas, al moverse continuamente y a altas velocidades, no sólo chocan entre sí, sino que también lo hace con las paredes del recipiente. Cada colisión contra la pared puede considerarse como una pequeñísima fuerza que se ejerce sobre ella. Se define entonces presión, como la fuerza que se ejerce por cada unidad de área, por consecuencia la presión de un gas estará dada por la suma de todos los choques que se producen sobre la unidad de área de pared.P= F/A.UNIDADES DE PRESIÓN: 1torr= 1mm Hg 1atm= 760torr = 760mmHg
- CANTIDAD DE SUSTANCIA (MOLES): La cantidad de sustancia que tiene un cuerpo se refiere a la masa que posee

- TEMAS A TRATAR EN QUÍMICA Y FÍSICA
- EXPERIMENTOS: 1. Experimentos comportamiento de gases y Ley de Boyle TEORIA Y EJERCICIOS
- http://www.quimicas.net/2015/05/ejemplos-de-la-ley-de-boyle.html 2. Demostrar la ley de Charles con un globo inflado http://www.quimicas.net/2015/05/ejemplos-de-la-ley-de-charles.html 3. LEY DE GAY LUSSAC 4. LEY COMBINADA DE LOS GASES: http://www.educaplus.org/game/ley-combinada-de-los-gases LEY COMBINADA DE LOS GASES
- 5. Ley de los gases ideales: http://www.educaplus.org/game/ley-de-los-gases-ideales La Ley general de los gases ideales surge como resultado del conocimiento obtenido de la Ley de Boyle, la Ley de Charles y la Ley de Avogadro. Si de la ecuación: se sustituye por , donde es el número de moles y es la constante universal de los gases ideales, entonces obtenemos la ecuación de la Ley General de los Gases Ideales: Esta ley es válida para la mayoría de los gases (dentro de ciertos límites de presión y temperatura) independientemente de su identidad química. La constante R es llamada Constante Universal de los Gases y es un factor de conversión fundamental. El valor de R depende de las unidades de P, V, T y n. La temperatura debe ser siempre expresada en la escala Kelvin (temperatura absoluta) La cantidad de gas n, se expresa normalmente en moles. Unidades para la constante universal de los gases R
 Problemas gases ideales.N TEMAS A TRATAR EN BIOLOGÍA:
Problemas gases ideales.N TEMAS A TRATAR EN BIOLOGÍA:
Gasometría arterial
Forma en que se realiza el examen
La sangre generalmente se toma de una arteria. En algunos casos, se puede usar la sangre de una vena.
La muestra de sangre puede tomarse de una de las siguientes arterias:
- La arteria radial en la muñeca.
- La arteria femoral en la ingle.
- La arteria braquial en el brazo.
El médico puede evaluar la circulación a la mano antes de sacar una muestra de sangre del área de la muñeca.
El médico introducirá una pequeña aguja a través de la piel hasta la arteria. La muestra se envía rápidamente a un laboratorio para su análisis con el fin de garantizar resultados precisos.
Preparación para el examen
No hay una preparación especial. Si está recibiendo oxigenoterapia, la concentración de oxígeno debe permanecer constante durante 20 minutos antes del examen.
Coméntele al médico si está tomando anticoagulantes, como ácido acetilsalicílico (aspirin).
Lo que se siente durante el examen
Cuando se introduce la aguja para extraer la sangre, algunas personas sienten un dolor moderado; otras sólo sienten un pinchazo o sensación de picadura. Posteriormente, puede haber algo de sensación pulsátil o un hematoma leve, los cuales pronto desaparecen.
Razones por las que se realiza el examen
Este examen se utiliza para evaluar enfermedades respiratorias y padecimientos que afectan los pulmones. Ayuda a determinar la efectividad de la oxigenoterapia. El examen también suministra información acerca del equilibro acidobásico del cuerpo, el cual puede revelar indicios importantes acerca del funcionamiento del pulmón y del riñón y del estado metabólico general del cuerpo.
Resultados normales
Valores a nivel del mar:
- Presión parcial de oxígeno (PaO2): 75 – 100 mmHg
- Presión parcial de dióxido de carbono (PaCO2): 38 – 42 mmHg
- pH de sangre arterial de 7.38 – 7.42
- Saturación de oxígeno (SaO2): 94 – 100%
- Bicarbonato (HCO3): 22 – 28 mEq/L
Nota: mEq/L = miliequivalentes por litro; mmHg = milímetro de mercurio.
A altitudes de 900 m (3,000 pies) y más, el valor de oxígeno es más bajo.
Los rangos de los valores normales pueden variar ligeramente entre diferentes laboratorios. Algunos laboratorios usan diferentes medidas o podrían evaluar diferentes muestras. Hable con el médico acerca del significado de los resultados específicos de su examen.
Significado de los resultados anormales
Los resultados anormales pueden deberse a enfermedades pulmonares, renales o metabólicas. Las lesiones en cabeza o cuello u otras lesiones que afecten la respiración también pueden llevar a resultados anormales.
Riesgos
Hay muy poco riesgo cuando el procedimiento se lleva a cabo correctamente. Las venas y las arterias varían en tamaño de un paciente a otro y de un lado del cuerpo a otro; por esta razón, puede ser más difícil obtener una muestra de sangre de algunas personas que de otras.
Otros riesgos asociados con el examen pueden ser:
- Sangrado en el sitio de la punción
- Problemas de flujo de sangre en el sitio de la punción (raros)
- Contusión en el sitio de la punción
- Demora en el sangrado en el sitio de la punción
- Desmayo o sensación de mareo
- Hematoma (acumulación de sangre debajo de la piel)
- Infección (un riesgo leve cada vez que se presenta ruptura de la piel) TEMAS A TRATAR EN CIENCIA TECNOLOGÍA Y MEDIO AMBIENTE Soldadura oxiacetilénica
1- Introducción: En la soldadura oxiacetilénica la fuente de calor está originada por la combustión del oxígeno y acetileno.
2. El acetileno (C2H2) es un gas altamente inflamable, incoloro y más ligero que el aire (densidad del acetileno, 0.907 kg/m3). De los gases combustibles, el que dispone de mayor poder calorífico es el acetileno (poder calorífico del acetileno, 11.600 kcal/kg), lo que permite alcanzar temperaturas de llama más elevada (superior a los 3.000 ºC) y posee una gran intensidad de llama y velocidad de combustión, por lo que es universalmente utilizado en muchos procesos industriales: soldadura y corte, tratamientos por calor, escarificado, enderezado, temple y revenido de partes mecánicas…
El proceso se origina por el intenso calor de la llama oxiacetilénica que eleva la temperatura del metal base, y que permite que el metal de aportación fluya fundido sobre el la superficie del metal base, que no llega a fundirse. La superficie del metal base debidamente calentada y químicamente limpia arrastra hacia el interior por atracción capilar la película de material de aporte, lo que a su vez origina el enfriamiento del metal base hasta que el metal de aporte se solidifique.
Esta humectación o mojado del metal base por parte de la película que forma el metal de aporte dependerá de la naturaleza de los metales a unir y del estado de sus superficies. En la práctica las superficies se van a presentar contaminadas por óxidos o grasas que van a impedir un correcto mojado.
Para obtener resultados satisfactorios es necesario recubrir o decapar las superficies de las piezas a unir con fundentes limpiadores.
2.2- Tipos de procesos en la soldadura oxiacetilénica: En la soldadura oxiacetilénica se diferencias dos procedimientos distintos, a saber:
– Soldadura por fusión: cuando los bordes de las piezas en contacto se funden por la acción de la llama oxiacetilénica. En este caso, también puede haber o no material de aporte. En caso de no utilizarse varilla de aporte, son los bordes de las piezas en contacto las que funden. Al fundirse los bordes, éstos fluyen en contacto, que tras enfriarse resulta todo un solo bloque de metal. Cuando se utiliza varilla de aporte, ésta deberá tener la misma composición que las piezas a unir.
– Soldadura fuerte y blanda: en este procedimiento las piezas a unir no llegan a fundir sus bordes, sino que se crean juntas de alta resistencia en la zona de contacto. Este tipo de procedimiento se divide a su vez en Soldadura Fuerte («Brazing» en inglés) o Soldadura Blanda («Soldering»). Las aleaciones ferrosas que fluyan a una temperatura máxima de 427ºC son utilizadas en la soldadura blanda, mientras que aquellas que fluyan a temperatura superiores a 427ºC serán utilizadas para la soldadura fuerte. En todo caso, la temperatura de trabajo siempre será inferior a la temperatura de fusión del metal base. La gran aplicación de este procedimiento es para aquellos materiales donde estas bajas temperaturas de trabajo evitan que se genere cambios estructurales por el efecto de las altas temperaturas.
2.3- Preparación de superficies
La limpieza de las superficies tiene por objeto la eliminación de cuerpos extraños que van a dificultar el correcto mojado del metal de aporte. Se podrán utilizar dos procedimientos:
• Limpieza mecánica;
• Limpieza química.
La limpieza química consiste en el empleo de determinados agentes limpiadores, llamados fundentes.
Los fundentes sirven para disolver o escorificar los óxidos que se forman sobre la superficie de diversos metales durante el proceso de calentado. Los fundentes suelen presentarse en forma de polvos, y en algunos casos, como líquidos.
Los fundentes presentan una temperatura de fusión más baja que la del metal de aporte. Cuando alcanzan esta temperatura, mojan o humectan la superficie de contacto y sirven también como indicador de temperatura para la aplicación del metal de aporte.
No existe un fundente universal para todos los usos, debido a que los óxidos de los diferentes metales y aleaciones varían mucho de propiedades físicas y químicas. Cada metal base o cada varilla de aportación requerirá el empleo de un fundente especial, según sus características. La elección del tipo de fundente deberá hacerse en todo caso consultando los catálogos de los suministradores.
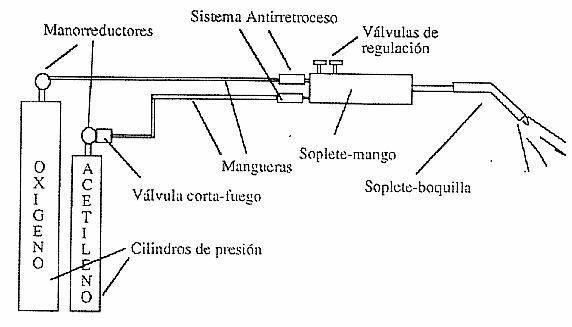
3- Equipo de soldadura
Adjunto se representa esquemáticamente el equipo de soldadura necesario,
CONTAMINACIÓN ATMOSFÉRICA TIPOS DE CONTAMINANTES

CONTAMINANTES PRIMARIOS
Los contaminantes primarios son aquellas sustancias contaminantes que se vierten directamente a la atmósfera, pueden venir de distintas fuentes, dando lugar a la contaminación convencional. Podemos agruparlos según su peculiaridad como puede ser su estado físico o los elementos químicos que tengan en común.
- Aerosoles (en los que se incluyen las partículas sedimentables y en suspensión y los humos).
- Óxidos de azufre, SOx.
- Monóxido de carbono, CO.
- Óxidos de nitrógeno, NOx.
- Hidrocarburos, Hn Cm.
- Ozono, O3.
- Anhídrido carbónico, CO2.
CONTAMINANTES SECUNDARIOS
Los contaminantes atmosféricos secundarios son los que se producen como consecuencia de las transformaciones y reacciones químicas y fotoquímicas, que sufren los contaminantes primarios en el seno de la misma. Las principales alteraciones atmosféricas producidas por los contaminantes secundarios son:



